Questão 1
(Fameca–SP) Compostos HF, NH3 e H2O apresentam elevados pontos de fusão e de ebulição quando comparados a H2S e HCl, por exemplo, devido:
a) às forças de van der Waals;
b) às forças de London;
c) às ligações de hidrogênio;
d) às interações eletrostáticas;
e) às ligações iônicas.
Questão 2
Relacione as colunas abaixo e indique quais são as principais forças intermoleculares (coluna I) que ocorrem entre as moléculas das substâncias moleculares listadas na coluna II.
Coluna I:
I- Ligação de hidrogênio;
II- Interação dipolo-dipolo;
III- Interação dipolo induzido-dipolo induzido.
Coluna II:
a) Amônia (NH3).
b) Água (H2O).
c) Acetaldeído (CH2O).
d) Bromo (Br2).
e) Cianeto de hidrogênio (HCN).
Questão 3
O gás presente nas bebidas gaseificadas é o dióxido de carbono (CO2). O aumento da pressão e o abaixamento da temperatura facilitam a dissolução do dióxido de carbono em água. Que tipo de interação intermolecular ocorre entre as moléculas de dióxido de carbono, entre as moléculas de água e entre as moléculas de dióxido de carbono e água, respectivamente?
a) Nos três casos ocorrem interações do tipo dipolo induzido-dipolo induzido.
b) dipolo induzido-dipolo induzido, ligações de hidrogênio, dipolo-dipolo induzido.
c) ligações de hidrogênio, ligações de hidrogênio, dipolo induzido-dipolo induzido.
d) ligações de hidrogênio, dipolo induzido-dipolo induzido, dipolo-dipolo induzido.
e) dipolo induzido-dipolo induzido, ligações de hidrogênio, ligações de hidrogênio.
Questão 4
(FGV-SP) O conhecimento das estruturas das moléculas é um assunto bastante relevante, já que as formas das moléculas determinam propriedades das substâncias como odor, sabor, coloração e solubilidade. As figuras apresentam as estruturas das moléculas de CO2, H2O, NH3, CH4, H2S e PH3.
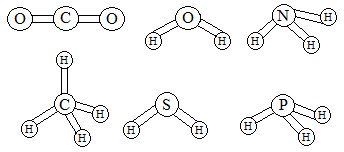
Estruturas de moléculas em exercícios sobre interações intermoleculares
Quanto às forças intermoleculares, a molécula que forma ligações de hidrogênio (pontes de hidrogênio) com a água é:
a) H2S.
b) CH4.
c) NH3.
d) PH3.
e) CO2.
Resposta Questão 1
Alternativa “c”.
Os compostos HF, NH3 e H2O estabelecem ligações de hidrogênio, que são interações intermoleculares muito fortes que ocorrem entre um átomo de hidrogênio e um átomo de flúor, nitrogênio ou oxigênio.
Resposta Questão 2
a) Amônia (NH3): I- Ligação de hidrogênio;
b) Água (H2O): I- Ligação de hidrogênio;
c) Acetaldeído (CH2O): II- Interação dipolo-dipolo;
d) Bromo (Br2): III- Interação dipolo induzido-dipolo induzido;
e) Cianeto de hidrogênio (HCN): II- Interação dipolo-dipolo;
Resposta Questão 3
Alternativa “b”.
Entre as moléculas de dióxido de carbono ocorrem interações do tipo dipolo induzido-dipolo induzido, pois o CO2 é uma molécula apolar. Mas quando duas moléculas apolares aproximam-se, os elétrons das eletrosferas dos átomos repelem-se, provocando um movimento dos elétrons, que se acumulam em uma única região. Desse modo, cria-se um dipolo na molécula de CO2, pois uma região fica com acúmulo de elétrons e carga negativa, e outra região fica com deficiência de elétrons e carga positiva, e assim elas atraem-se fracamente.
Já as moléculas de água realizam ligações de hidrogênio entre o hidrogênio de uma molécula e o oxigênio de outra.
As moléculas de água são polares, portanto, já possuem um dipolo, ou seja, uma região carregada negativamente e outra positivamente, que interage com as moléculas de CO2 que foram induzidas a ter um dipolo. Por isso, é uma interação entre o dipolo da água e o dipolo induzido do CO2.
Resposta Questão 4
Alternativa “c”.
Para formar pontes de hidrogênio com a H2O, é necessário que a molécula possua átomos de hidrogênio ligados a elementos muito eletronegativos, como o flúor, oxigênio e o nitrogênio. A única molécula que satisfaz esse requisito é a amônia (NH3).



