Questão 1
Analise o diagrama fornecido a seguir:
A + B → C + D
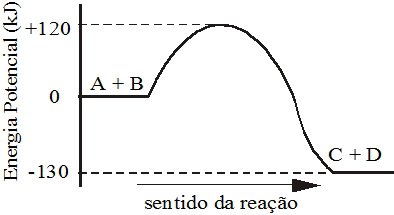
Assinale a alternativa correta:
a) A energia de ativação do processo tem o valor de 250 KJ.
b) A energia referente ao complexo ativado é igual a 120 KJ.
c) A energia dos reagentes é igual a 120 KJ.
d) A energia dos produtos é igual a 120 KJ.
e) Todas as afirmativas estão erradas.
Questão 2
O diagrama fornecido a seguir se refere à combustão da substância etanol:
C2H6O + 3 O2 → 2 CO2 + 3 H2O
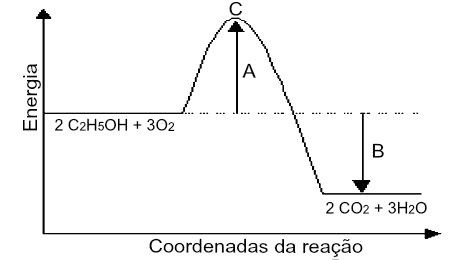
a) A representa o complexo ativado.
b) B representa a energia de ativação.
c) C representa a formação do produto.
d) A reação representada é endotérmica.
e) C representa o complexo ativado.
Questão 3
(Mackenzie-SP)
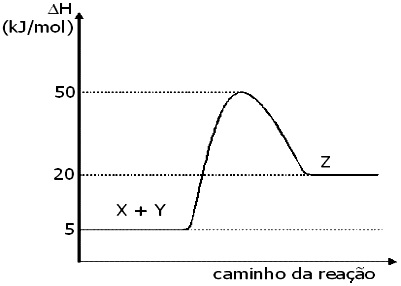
O gráfico acima representa a reação:
X + Y → Z
Os valores do ΔH e da energia de ativação, em kJ/mol, são, respectivamente,
a) + 50 e 20.
b) + 15 e 45.
c) + 30 e 20.
d) + 5 e 20.
e) + 25 e 55.
Questão 4
(Mackenzie-SP) Considerando o diagrama da reação genérica A + B → C + D, fazem-se as afirmações:
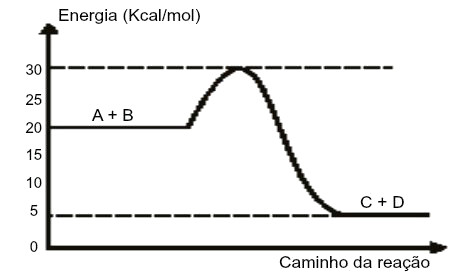
I. a reação é exotérmica.
II. o ΔH da reação direta é igual a –15 kcal/mol.
III. a energia de ativação da reação direta é igual a + 25 kcal/mol.
IV. a reação direta ocorre com liberação de calor.
São corretas, somente:
a) I, II e IV.
b) I e III.
c) III e IV.
d) II e IV.
e) I e II.
Resposta Questão 1
Letra b). A letra “a” está errada porque a energia de ativação sempre é a diferença entre a energia do complexo ativado (ponto mais alto da curva, 120 KJ) e a energia dos reagentes (OKJ). A letra “c” está errada porque a energia dos reagentes é igual a 0 KJ. A letra “d” está errada porque a energia dos produtos é igual a -130 KJ.
Resposta Questão 2
Letra e). A letra “a” está errada porque o item A representa a energia de ativação (parte dos reagentes em direção ao complexo ativado). A letra “b” está errada porque o item B representa a variação da entalpia (parte dos reagentes em direção aos produtos). A letra “c” está errada porque C representa o complexo ativado. A letra “d” está errada porque o processo é exotérmico, já que os reagentes apresentam mais energia que os produtos.
Resposta Questão 3
Letra b). Para calcular o valor do ΔH, basta utilizar a expressão:
ΔH = Hp- Hr
ΔH = 20 - 5
ΔH = 15 KJ
Hp (entalpia dos produtos) e Hr (entalpia dos reagentes)
Já a energia de ativação sempre parte dos reagentes (5 KJ) em direção ao complexo (50 KJ). Para calculá-la, basta realizar a diferença entre o complexo e od reagentes:
50-5 = 45 KJ
Resposta Questão 4
Letra a). O item I está correto porque a entalpia dos reagentes (A e B) é maior que a dos produtos (C e D), o que caracteriza um processo exotérmico. O item II está correto porque, para calcular o ΔH, basta utilizar a seguinte expressão:
ΔH = Hp- Hr
ΔH = 5 - 20
ΔH = -15 KJ
Hp (entalpia dos produtos) e Hr (entalpia dos reagentes)
O item III está errado porque, para calcular a energia de ativação, sempre partimos dos reagentes (20 KJ) em direção ao complexo (30 KJ). Para calculá-la, basta realizar a diferença entre complexo e reagentes:
30-20 = 10 KJ



