Questão 1
A distribuição eletrônica do bário (Z=56) na ordem crescente de energia é:
a) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s2
b) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2
c) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f12
d) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f10
Questão 2
Ao se realizar a distribuição eletrônica do titânio, que possui número atômico igual a 22, descobre-se que o seu subnível mais energético e os elétrons distribuídos nele são dados por:
a) 3p3
b) 3p5
c) 4s2
d) 3d2
e) 4p6
Questão 3
Qual a distribuição eletrônica em camadas do átomo 2656Fe?
a) 2 – 8 – 10 – 2.
b) 2 – 8 – 12.
c) 2 – 8 – 8 – 4.
d) 2 – 8 – 18 – 18 – 8 – 2.
e) 2 – 8 – 14 – 2.
Questão 4
(Unifor-CE) O átomo de um elemento químico tem 14 elétrons no 3º nível energético (n = 3). O número atômico desse elemento é:
a) 14
b) 16
c) 24
d) 26
e) 36
Questão 5
(FEI-SP) A configuração eletrônica de um átomo neutro no estado fundamental é 1s2 2s2 2p6 3s2 3p5. O número de orbitais vazios remanescentes no nível principal M é:
a) 0
b) 1
c) 5
d) 6
e) 10
Questão 6
(Unaerp) O fenômeno da supercondução de eletricidade, descoberto em 1911, voltou a ser objeto da atenção do mundo científico com a constatação de Bednorz e Müller de que materiais cerâmicos podem exibir esse tipo de comportamento, valendo um prêmio Nobel a esses dois físicos em 1987. Um dos elementos químicos mais importantes na formulação da cerâmica supercondutora é o ítrio:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d1. O número de camadas e o número de elétrons mais energéticos para o ítrio, serão, respectivamente:
a) 4 e 1.
b) 5 e 1.
c) 4 e 2.
d) 5 e 3.
e) 4 e 3.
Resposta Questão 1
Alternativa “b”.
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2
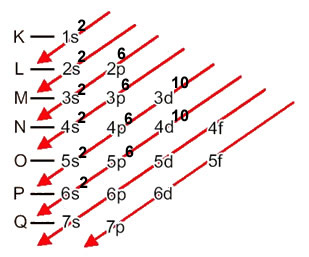
Distribuição eletrônica do bário no diagrama de Pauling
Resposta Questão 2
Alternativa “d”.
A distribuição eletrônica do titânio em ordem energética crescente é: 1s2 2s2 2p6 3s2 3p6 4s2 3d2. Portanto, o seu subnível mais energético é o último a ser preenchido: 3d2:
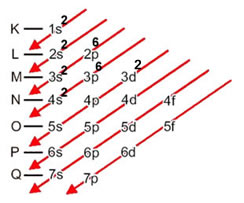
Distribuição eletrônica do titânio no diagrama de Pauling
Apenas para tirar quaisquer dúvidas, o subnível 4s2 é o mais externo e não o mais energético.
Resposta Questão 3
Alternativa “e”.
Pelo diagrama mostrado logo mais abaixo, você poderá ver que em cada camada a quantidade de elétrons é:
1ª camada: K = 2;
2ª camada: L = 8;
3ª camada: M = 14;
4ª camada: N = 2;
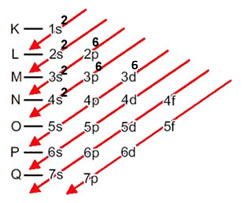
Distribuição eletrônica do ferro
Resposta Questão 4
Alternativa “d”.
O 3º nível energético é M, então, basta realizar a distribuição eletrônica, seguindo a ordem dada pelas setas, até que haja 14 elétrons nesse nível (2 + 6 + 6):

Distribuição eletrônica de 14 elétrons no terceiro nível do diagrama de Pauling
Somando todos os elétrons distribuídos, temos que o total é igual a 26.
Resposta Questão 5
Alternativa “c”.
O nível M é o terceiro, então, se olharmos esse nível, temos que os orbitais 3s e 3p estão preenchidos com elétrons, restando os 5 vazios do subnível 3d:
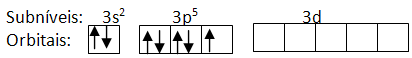
Subníveis e orbitais do nível M
Resposta Questão 6
Alternativa “b”.
Pela distribuição eletrônica mostrada no enunciado (1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d1), vemos que os elétrons foram distribuídos até a camada 5 (5s2). Visto que essa distribuição já está na ordem energética crescente, o subnível mais energético é o 4d que possui 1 elétron.



