Questão 1
(PUC-SP) Um estudante pretende separar os componentes de uma amostra contendo três sais de
chumbo II: Pb(NO3)2, PbSO4 e PbI2. Após analisar a tabela de solubilidade abaixo,
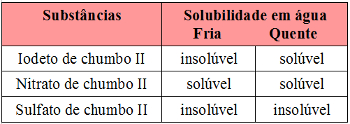
Solubilidade de sais de chumbo
ele propôs o seguinte procedimento:
“Adicionar água destilada em ebulição à mistura, agitando o sistema vigorosamente. Filtrar a suspensão resultante, ainda quente. Secar o sólido obtido no papel de filtro; este será o sal A. Recolher o filtrado em um béquer, deixando-o esfriar em banho de água e gelo. Proceder a uma nova filtração e secar o sólido obtido no papel de filtro; este será o sal B. Aquecer o segundo filtrado até a evaporação completa da água; o sólido resultante será o sal C”.
Os sais A, B e C são, respectivamente,
a) Pb(NO3)2, PbSO4 e PbI2.
b) PbI2, PbSO4 e Pb(NO3)2.
c) PbSO4, Pb(NO3)2 e PbI2.
d) PbSO4, PbI2 e Pb(NO3)2.
e) Pb(NO3)2, PbI2 e PbSO4.
Questão 2
Classifique os sais da coluna I segundo a natureza de seus íons, que está apontada na coluna II:
Coluna I: Coluna II:
A) NH4Cl I. Sal neutro.
B) CuSO4 . 5 H2O II. Sal básico.
C) KNaSO4 III. Sal ácido.
D) KAl(SO4)2 . 12 H2O IV. Sal duplo.
E) NaCl V. Sal hidratado.
F) NaOOCCH3 VI. Alúmen.
a) A-III; B-VI; C-IV; D-V; E-I; F-II.
b) A-II; B-V; C-IV; D-VI; E-III; F-I.
c) A-III; B-V; C-IV; D-VI; E-I; F-II.
d) A-II; B-I; C-VI; D-IV; E-III; F-V.
e) A-II; B-V; C-IV; D-VI; E-I; F-III.
Questão 3
(ITA-SP) São pouco solúveis em água os seguintes pares de sais:
a) BaCl2 e PbCl2.
b) MgSO4 e BaSO4.
c) PbSO4 e Pb(NO3)2.
d) K2CrO4 e Na2CrO4.
e) AgBr e PbS.
Questão 4
Qual das alternativas a seguir indica uma equação química que apresenta um hidrogenossal que é solúvel em água:
a) HCl + Ca(OH)2 → Ca(OH)Cl + H2O
b) H2SO4 + Al(OH)3 → Al2(SO4)3 + H2O
c) HCN + NH4OH → NH4CN + H2O
d) H3BO3 + Ca(OH)2 →Ca3(BO3)2- + H2O
e) HCl + AgOH → AgCl + H2O
Resposta Questão 1
Alternativa “d”.
Pelo procedimento citado, o sal A é insolúvel em água quente. Pela tabela, vemos que o único assim é o sulfato de chumbo II: PbSO4.
O sal B é solúvel em água quente e insolúvel em água fria (cristaliza com o resfriamento da água usada na dissolução): PbI2.
O sal C é solúvel tanto em água quente quanto em água fria, sendo, então, o nitrato de chumbo II: Pb(NO3)2. Ele só aparece como sólido quando a água de sua dissolução é totalmente vaporizada.
Resposta Questão 2
Alternativa “c”.
A) NH4Cl → III. Sal ácido.
Formado por uma base fraca e um ácido forte:
Cátion → NH42+ (vem do hidróxido de amônio, NH4OH, uma base fraca);
Ânion → Cl- (vem do ácido clorídrico, HCl, um ácido forte).
Quando esse sal é adicionado à água, o seu cátion oriundo de uma base fraca sofre hidrólise e gera íons H3O+ (aq), o que torna a solução ácida.
B) CuSO4 . 5 H2O → V. Sal hidratado.
É penta-hidratado, com moléculas de água em proporções definidas que ficam no retículo cristalino do sal no estado sólido.
C) KNaSO4 → IV. Sal duplo.
Em solução aquosa, libera dois cátions: K+ e Na+.
D) KAl(SO4)2 . 12 H2O → VI. Alumen.
É formado por dois cátions (K+ e Al3+), sendo um monovalente (com carga +1) e o outro trivalente (com carga +3), por um único ânion (o sulfato (SO42-)) e por água de cristalização.
E) NaCl → I. Sal neutro.
Esse sal foi formado pela reação de um ácido e uma base fortes:
Cátion → Na+ (vem do hidróxido de sódio, NaOH, uma base forte);
Ânion → Cl- (vem do ácido clorídrico, HCl, um ácido forte).
Em água, ele não altera o pH do meio.
F) NaOOCCH3 → II. Sal básico.
Foi formado por um ácido fraco e uma base forte:
Cátion → Na+ (vem do hidróxido de sódio, NaOH, uma base forte);
Ânion → CH3COO– (vem do ácido etanoico, CH3COOH, H2CO3, um ácido fraco).
O ânion acetato (CH3COO–) hidrolisa-se em meio aquoso e forma o ácido acético e íons hidroxila (OH–), o que torna a solução básica.
Resposta Questão 3
Alternativa “e”.
a) Os cloretos costumam ser solúveis, exceto os de prata, mercúrio I, ouro, cromo III e de chumbo II (PbCl2). Esse último aparece na alternativa, mas o cloreto de bário (BaCl2) é solúvel em água.
b) Os sulfatos costumam ser solúveis, exceto os de estrôncio, cálcio, prata, mercúrio I, mercúrio II e de bário (BaSO4). Esse último aparece na alternativa, mas o sulfato de magnésio ( MgSO4) é solúvel em água.
c) O sulfato de chumbo II (PbSO4) é solúvel e todos os nitratos são solúveis, incluindo o nitrato de chumbo II (Pb(NO3)2) citado na alternativa.
d) Os cromatos são insolúveis.
e) Os brometos são solúveis, mas o de prata é uma exceção. Já os sulfetos são insolúveis. Assim, o AgBr e o PbS são pouco solúveis em água.
Resposta Questão 4
Alternativa “b”.
b) H2SO4 + Al(OH)3 → Al2(SO4)3 + H2O
Esse sal é formado por um ácido forte (ácido sulfúrico - H2SO4) e por uma base fraca (hidróxido de alumínio - Al(OH)3 ), formando um sal ácido ou hidrogenossal. Ele é também solúvel em água por ser um sulfato de alumínio.



