Questão 1
Certa máquina térmica recebe 500 J de calor e realiza um trabalho de 125 cal. Sendo 1 cal = 4 J, marque a alternativa correta.
a) Essa máquina contraria a primeira lei da Termodinâmica.
b) A máquina não contraria a segunda lei da Termodinâmica.
c) O rendimento dessa máquina é de 25%.
d) A máquina não contraria a primeira lei da Termodinâmica, que trata sobre a conservação da energia.
e) Como o rendimento da máquina é de 25%, podemos afirmar que ela não contraria a primeira lei da Termodinâmica.
Questão 2
(ITA) Uma máquina térmica opera segundo o ciclo JKLMJ mostrado no diagrama T-S da figura.
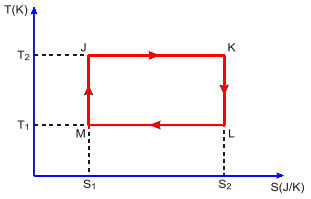
Pode-se afirmar que:
a) processo JK corresponde a uma compressão isotérmica.
b) o trabalho realizado pela máquina em um ciclo é W = (T2 – T1)(S2 – S1).
c) o rendimento da máquina é dado por η = 1 – T2/T1.
d) durante o processo LM, uma quantidade de calor QLM = T1(S2 – S1) é absorvida pelo sistema.
e) outra máquina térmica que opere entre T2 e T1 poderia eventualmente possuir um rendimento maior que a desta.
Questão 3
(UNAMA) Um motor de Carnot cujo reservatório à baixa temperatura está a 7,0°C apresenta um rendimento de 30%. A variação de temperatura, em Kelvin, da fonte quente a fim de aumentarmos seu rendimento para 50% será de:
a) 400
b) 280
c) 160
d) 560
Questão 4
A respeito da primeira lei da Termodinâmica, marque a alternativa incorreta:
a) Em uma transformação isotérmica, a variação da energia interna é nula.
b) A primeira lei da Termodinâmica trata da conservação da energia.
c) Em uma transformação isocórica, não haverá realização de trabalho.
d) Em uma transformação adiabática, o trabalho será realizado sobre gás quando a variação da energia interna é positiva.
e) A primeira lei da Termodinâmica diz que o calor fornecido a um gás é igual à soma do trabalho realizado pelo gás e a sua variação da energia interna.
Resposta Questão 1
LETRA “D”
O trabalho de 125 cal corresponde a 500 J (125 cal x 4J = 500 J), logo, toda a energia recebida pela máquina é convertida em trabalho. Isso não contraria a primeira lei da Termodinâmica, que prevê esse tipo de situação para uma transformação isotérmica, mas contraria a segunda lei, pois é impossível haver máquinas térmicas com rendimento igual a 100%.
Resposta Questão 2
LETRA “B”
O gráfico dado na questão é de temperatura versus entropia e mostra um ciclo no sentido horário operado por uma máquina térmica. Sendo assim, podemos analisar cada uma das alternativas:
A) ERRADO: No processo JK, ocorre aumento de entropia, o que indica que o sistema recebeu calor.
B) CORRETO: Em um ciclo, o trabalho é dado pela área do gráfico.
c) ERRADO: Nesse caso, teríamos η = 1 – T1/T2.
d) ERRADO: Durante o processo LM, há diminuição de entropia, o que indica perda de calor.
e) ERRADO: Outra máquina operando sob o mesmo ciclo realizaria o mesmo trabalho.
Resposta Questão 3
LETRA “C”
Sendo 7,0 °C a temperatura da fonte fria e aplicando o rendimento de Carnot para o rendimento de 30%, teremos:
T2 = 7 °C = 7+273 = 280 K
η = 1 – T2/T1.
0,3 = 1 – 280/T1
280/T1 = 1 – 0,3
280/T1 = 0,7
T1 = 280 ÷ 0,7
T1 = 400 K
Para o rendimento de 50%, mantendo a mesma temperatura da fonte fria, teremos:
η = 1 – T2/T1
0,5 = 1 – 280/T1
280/T1 = 1 – 0,5
280/T1 = 0,5
T1 = 280 ÷ 0,5
T1 = 560 K
A variação da temperatura da fonte quente necessária para que o rendimento aumente de 30% para 50% é de 160 K.
560 – 400 = 160 K
Resposta Questão 4
LETRA “E”
De acordo com a primeira lei da Termodinâmica, temos:
Portanto, a quantidade de calor fornecida a um gás é igual a soma do trabalho realizado pelo gás (τ > 0) e a variação da energia interna.



