Questão 1
Qual é o conjunto dos quatro números quânticos que caracteriza o elétron mais energético do 35Br?
a) n = 3, l = 2, m = +2, s = +1/2.
b) n = 4, l = 0, m = 0, s = +1/2.
c) n = 3, l = 1, m = +2, s = +1/2.
d) n = 4, l = 1, m = 0, s = +1/2.
e) n = 4, l = 3, m = +2, s = +1/2.
Questão 2
(UEPI) Sobre o elemento químico vanádio, de número atômico 23, são feitas as seguintes afirmações:
I. A camada de valência do vanádio possui três (3) elétrons;
II. Possui onze (11) elétrons na terceira camada eletrônica;
III. Os quatro números quânticos para os elétrons da última camada são : 3 ; 2 ; 0 ; + 1/2;
IV. A camada de valência do vanádio possui dois (2) elétrons.
Indique a alternativa correta:
a) somente as afirmações II e IV estão corretas.
b) somente as afirmações I e II estão corretas.
c) somente as afirmações III e IV estão corretas.
d) somente as afirmações I e III estão corretas.
e) somente as afirmações I e IV estão corretas.
Questão 3
(Uespi) Dado o átomo 17X, o conjunto dos quatro números quânticos para o 11º elétron do subnível p é:
a) 3, 1, 0 e – 1/2.
b) 3, 1, 1 e – 1/2.
c) 3, 1, 0 e + 1/2.
d) 3, 2, 0 e – 1/2.
e) 3, 2, 0 e + 1/2.
Questão 4
Um elétron na camada O está no subnível s. Quais são os valores de n e ??
a) 3 e 0.
b) 4 e 1.
c) 5 e 0.
d) 5 e 1.
e) 6 e 0.
Resposta Questão 1
Alternativa “d”.
Primeiro realizamos a distribuição eletrônica no Diagrama de Pauling dos 35 elétrons do bromo. Feito isso, encontramos a seguinte distribuição em ordem de energia: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5.
Veja que o subnível mais energético é o último a ser preenchido, ou seja, o 4p5.
*Temos então que o nível é o N ou 4, ou seja, o número principal é: n =4.
*O subnível é o p, então, o número quântico secundário é: l = 1.
* Visto que são cinco elétrons e queremos saber o do quinto elétron, que foi o último a ser preenchido e que é o mais energético, vamos realizar a distribuição deles nos orbitais para descobrir o número quântico magnético e o spin. Lembrando que primeiro vamos preencher com todas as setas para cima e depois preenchar com as setas para baixo, obedecendo à regra de Hund.
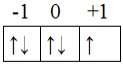
Distribuição eletrônica nos orbitais do subnível mais energético do bromo
A última seta a ser preenchida, que é o elétron mais energético, ficou no 0, então, o valor do número quântico magnético é: m = 0.
*Visto que a seta está para baixo, temos por convenção que o número quântico spin é: s = +1/2.
Resposta Questão 2
Alternativa “a”.
I. Falsa. A camada de valência do vanádio não possui três (3) elétrons, mas sim dois (2), porque a camada de valência é a mais externa, e não a mais energética. Veja pela distribuição eletrônica dos 23 elétrons em ordem de energia do vanádio que o subnível mais externo é o 4s2 e o mais energético é o 3d3: 1s2 2s2 2p6 3s2 3p6 4s2 3d3.
II. Verdadeira. Possui onze (11) elétrons na terceira camada eletrônica: 3s2 3p6 3d3 (2 + 6 + 3 = 11).
III. Falsa. Os quatro números quânticos para os elétrons da última camada não são : 3 ; 2 ; 0 ; + ½.
Se é a última camada, é a camada mais externa, ou seja, refere-se ao 4s2 , cujos números quânticos são: 4; 0; 0 ; + ½. Os valores apresentados na afirmativa são os números quânticos do subnível mais energético, 3d3.
IV. Verdadeira. A camada de valência do vanádio possui dois (2) elétrons, conforme explicado no item I.
Resposta Questão 3
Alternativa “c”.
O enunciado disse que o número atômico é 17. Assim, fazendo a distribuição em ordem crescente de energia, temos que o subnível mais energético é o 3p5: 1s2 2s2 2p6 3s2 3p5.
Mas foi dito também que o que se deseja são os números quânticos para o 11º elétron do subnível “p”, ou seja, no subnível p, há: 2p6 e 3p5 = 6 + 5 = 11.
Assim, temos que se refere realmente ao subnível 3p5:
*O nível é o M ou 3, ou seja, o número principal é: n = 3.
*O subnível é o p, então, o número quântico secundário é: ? = 1.
* Visto que são cinco elétrons e queremos saber o do quinto elétron, que foi o último a ser preenchido e que é o mais energético, vamos realizar a distribuição deles nos orbitais para descobrir o número quântico magnético e o spin. Lembrando que primeiro vamos preencher com todas as setas para cima e depois preencher com as setas para baixo, obedecendo à regra de Hund.
.jpg)
Distribuição eletrônica nos orbitais do subnível mais energético
A última seta a ser preenchida, que é o elétron mais energético, ficou no 0, então, o valor do número quântico magnético é: m = 0.
*Visto que a seta está para baixo, temos por convenção que o número quântico spin é: s = +1/2.
Resposta Questão 4
Alternativa “c”.
A camada O é o quinto nível eletrônico, então, o número quântico principal é: n = 5;
O subnível é o s, então o valor do número quântico secundário ou azimutal é: l = 0.



